NRG-HN002: A Randomized Phase II Trial for Patients With p16-Positive, Non-Smoking-Associated, Locoregionally Advanced oropharyngeal Cancer
S.S. Yom, P. Torres-Saavedra, J.J. Caudell, J.N. Waldron, M.L. Gillison, M.T.Truong, R. Jordan, R. Subramaniam, M. Yao, C. Chung, J.L. Geiger, J. Chan,B. O’Sullivan, D.M. Blakaj, L.K. Mell, W.L. Thorstad, C.U. Jones, R.N. Banerjee,C.E. Lominska, and Q.T. Le.
Il est désormais admis que le virus HPV est un facteur de risque des cancersdes VADS, particulièrement de la sphère oropharyngée, mais aussi un facteurpronostique majeur faisant des patients non (ou faiblement) fumeursHPV+, une catégorie de malades dont la survie à 5 ans est triplée en comparaisonavec les patients fumeurs HPV- (1,2).
Sur ces constatations, et devant la morbidité relative de l’associationradiochimiothérapie, plusieurs protocoles dits de « dé-intensification »ont émergé, sans qu’aucun ne soit encore admis comme référencedans cette population grandissante de tumeurs HPV+. On pourrait lister :diminution des doses de radiothérapie (+/- chimiothérapie d’induction,ECOG-1308), remplacement du Cisplatine par le Cetuximab (De-ESCALaTE &RTOG-1016, (3,4)), radiothérapie exclusive (présente étude), chirurgie suivie deradiochimiothérapie « faible dose » (ECOG-3311, Pathos) ou chirurgie seule.
La présente étude (NRG-HN002) est une phase II randomisée multicentrique(62 institutions) comparant, chez des patients porteurs de cancers oropharyngésp16+ & <10PA & T1-2 N1-2b ou T3 N0-2b (AJCC 7ème ed) :
- Association RadioThérapie-ChimioThérapie (RTCT) : IMRT 60 Gy normofractionnée+ Cisplatine hebdomadaire 40 mg/m²,
- vs radiothérapie exclusive : IMRT 60 Gy modérément accélérée(6 fractions / semaine).
Le design de cette étude visait à sélectionner la stratégie offrant la meilleuresurvie sans progression sans altération de la qualité de vie (MDADI compositescore), co-critères de jugement principaux.
308 patients ont été randomisés (306 analysés) de 10/2014 à 02/2017 etrépartis comme suit : 157 RTCT et 149 radiothérapies exclusives. La sélectiondes patients était équilibrée et on notera : 69.6% de non-fumeurs (0PA), 52.6%de tumeurs amygdaliennes, 48% de stades T2 et 61.4% N2b.
La compliance aux traitements était excellente dans les 2 bras puisque 97.8% despatients ont achevé leur radiothérapie et, dans le bras RTCT, 80.9% ont reçu aumoins 5 cycles de Cisplatine et 72.6% une dose cumulée ≥ 200 mg/m².
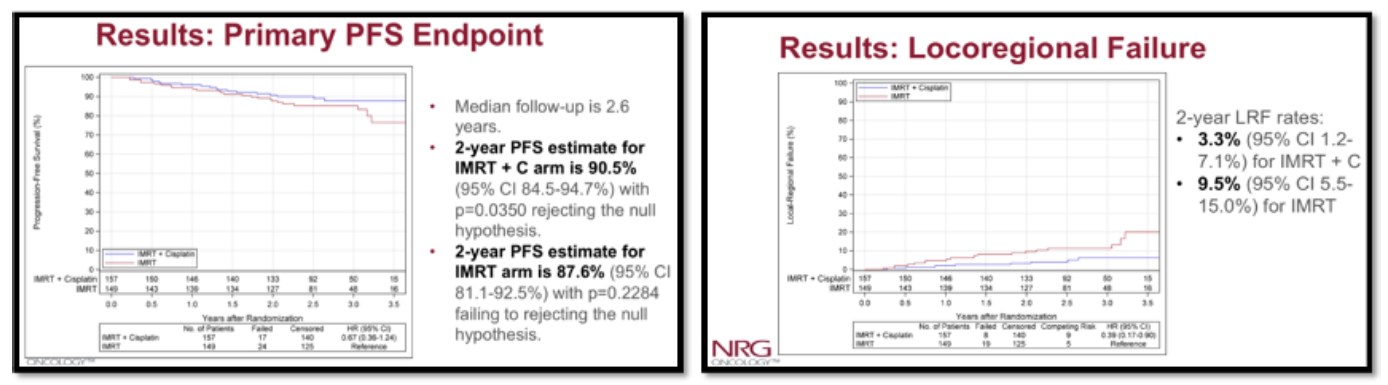
Avec un suivi médian de 2.6 ans, le bras RTCT offrait une survie sans progressionà 2 ans de 90.5% (95% CI 84.5-94.7%, p 0.035), supérieure aubras radiothérapie seule relevée à 87.6% (95% CI 81.1-92.5%, p 0.2284)(cf figures). Les récidives loco-régionales ont concerné 7 patients en RTCT et16 patients en radiothérapie exclusive (dont 10 récidives locales « pures »).
Les toxicités aigues G3-4 ont concerné 79.6% des patients en RTCT et 52.3%des patients en radiothérapie exclusive ; les toxicités tardives G3-4 étantrespectivement de 21.3% et 18.1%. A 1 an, la proportion de patients nécessitantun support nutritionnel entéral ne différait pas entre les 2 bras (3 vs 2%)et le score MDADI était relevé à 85.3 pour le bras RTCT et 81.76 pour le brasradiothérapie exclusive (p 0.0755).
Les auteurs concluent que l’association RTCT répond aux deux co-critères,à la différence de la radiothérapie exclusive qui n’atteint pas le seuil desurvie sans progression exigé initialement par les statisticiens. Cette étudedevrait déboucher sur une phase III (NRG-HN005) comparant : RTCT 70 Gyvs RTCT 60 Gy vs RT-Nivolumab 60 Gy, les doses de Cisplatine vogueraientalors vers 100 mg/m² J1-22…
En discussion, il a été pointé que cette étude comparait « dé-intensification »vs « dé-intensification » et que la « dé-intensification » l’a emporté… Le standardactuel doit rester, en dehors d’essai clinique, l’association RTCT à 70 Gy.Pour terminer, une couverture vaccinale digne de ce nom permettra peutêtrede rendre, dans les décennies à venir, ce type d’étude obsolète (5)
Références
1: Lassen P, Lacas B, Pignon JP, Trotti A, Zackrisson B, Zhang Q, Overgaard J,Blanchard P; MARCH Collaborative Group. Prognostic impact of HPV-associatedp16-expression and smoking status on outcomes following radiotherapy fororopharyngeal cancer: The MARCH-HPV project. Radiother Oncol. 2018Jan;126(1):107-115.
2: Ang KK, Harris J, Wheeler R, Weber R, Rosenthal DI, Nguyen-Tân PF, Westra WH,Chung CH, Jordan RC, Lu C, Kim H, Axelrod R, Silverman CC, Redmond KP, GillisonML. Human papillomavirus and survival of patients with oropharyngeal cancer.N Engl J Med. 2010 Jul 1;363(1):24-35.
3: Mehanna H, Robinson M, Hartley A, Kong A, Foran B, Fulton-Lieuw T, Dalby M,Mistry P, Sen M, O'Toole L, Al Booz H, Dyker K, Moleron R, Whitaker S, Brennan S,Cook A, Griffin M, Aynsley E, Rolles M, De Winton E, Chan A, Srinivasan D, Nixon I,Grumett J, Leemans CR, Buter J, Henderson J, Harrington K, McConkey C, Gray A,Dunn J; De-ESCALaTE HPV Trial Group. Radiotherapy plus cisplatin or cetuximabin low-risk human papillomavirus-positive oropharyngeal cancer (De-ESCALaTEHPV): an open-label randomised controlled phase 3 trial. Lancet. 2019 Jan5;393(10166):51-60.
4: Gillison ML, Trotti AM, Harris J, Eisbruch A, Harari PM, Adelstein DJ, Sturgis EM,Burtness B, Ridge JA, Ringash J, Galvin J, Yao M, Koyfman SA, Blakaj DM, Razaq MA,Colevas AD, Beitler JJ, Jones CU, Dunlap NE, Seaward SA, Spencer S, GallowayTJ, Phan J, Dignam JJ, Le QT. Radiotherapy plus cetuximab or cisplatin in humanpapillomavirus-positive oropharyngeal cancer (NRG Oncology RTOG 1016): arandomised, multicentre, non-inferiority trial. Lancet. 2019 Jan 5;393(10166):40-50.
ALEXANDRE COUTTE,
Radiothérapie,
Amiens


